蛋白质印迹法疑难排解指南
精心设计的实验,具有适当的控制、处理和条件,通常是获得改进结果的第一步。要了解有关蛋白质印迹实验的更多信息,请查看我们的蛋白质印迹实验指南。
| 问题 | 可能的原因 | 建议 |
|---|---|---|
信号弱或无信号 | 重复使用预稀释的抗体 | 不建议重复使用稀释的抗体,因为稀释后的抗体稳定性较差,并且存放太久的稀释缓冲液容易产生微生物或真菌污染。我们建议始终使用新鲜稀释的抗体,以获得最佳结果。 |
组织或细胞系中的蛋白表达水平低 | 我们建议使用 BioGPS 或 Human Protein Atlas 等表达谱分析工具以及科学文献,来检查细胞或动物组织是否预期能够充分表达目的靶蛋白。我们始终建议加入已知的阳性对照,以确认实验结果。如需了解我们许多抗体的推荐对照列表,请参阅我们按靶标划分的对照处理表。 对于全细胞提取物,每个泳道建议上样至少 20-30 μg 的蛋白,以便检测全组织提取物中的总/未修饰靶标。然而,通常需要将总蛋白上样量增加到每个泳道至少 100 μg,以检测全组织提取物中的修饰靶标(如磷酸化和切割靶标)。当组织中只有一小部分细胞包括翻译后修饰靶标时,全组织提取物可能需要上样更多蛋白。在细胞提取物中加入蛋白酶和磷酸酶抑制剂,对于避免蛋白降解和维持蛋白产率至关重要。我们建议往裂解缓冲液中加入亮抑酶肽(最终浓度为 1.0 μg/ml)和 PMSF (#8553) 作为蛋白酶抑制剂。还可以使用 Protease Inhibitor Cocktail (100X) (#5871) 或 Protease/Phosphatase Inhibitor Cocktail (100X) (#5872)。 | |
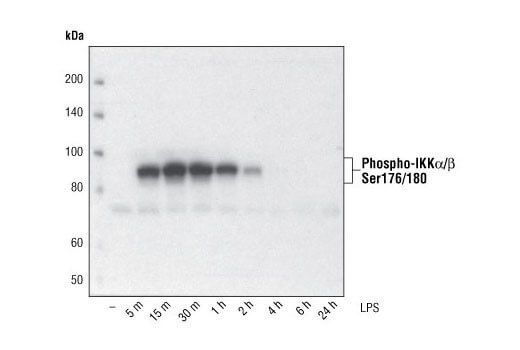
磷酸化或修饰蛋白的水平低 | 在未处理的细胞系或组织中,许多翻译后修饰蛋白的基底表达水平较低。我们建议使用 PhosphoSitePlus 查找提及您特定修饰位点的低引用率论文,或使用我们按靶标划分的对照处理表查找某种处理方法以及可很好地作为阳性对照的细胞系或组织的例子。 在细胞提取物中加入蛋白酶和磷酸酶抑制剂,对于避免蛋白降解和维持蛋白产率至关重要。应将焦磷酸钠(最终浓度为 2.5 mM)和 β-甘油磷酸盐(最终浓度为 1.0 mM)作为丝氨酸/苏氨酸磷酸酶抑制剂加入裂解缓冲液中。应加入正钒酸钠(最终浓度为 2.5 mM)以抑制酪氨酸磷酸酶。还可以使用 Protease Inhibitor Cocktail (100X) (#5871) 或 Protease/Phosphatase Inhibitor Cocktail (100X) (#5872)。 | |
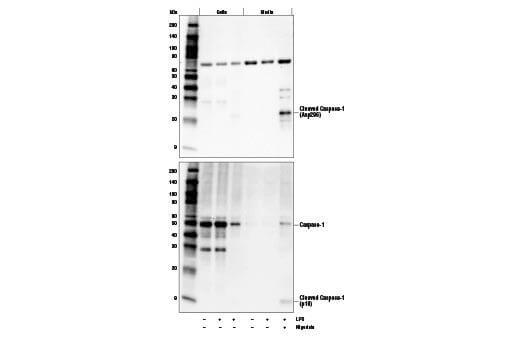
分泌蛋白 | 某些靶蛋白是由细胞分泌的,因此在全细胞提取物中无法可靠地检测到。细胞培养基使用丙酮进行沉淀,或进行浓缩,以检测分泌的靶标。在某些情况下,可使用 Brefeldin A (#9972) 等化学调节剂抑制细胞分泌目的蛋白。 | |
抗体灵敏度和反应性 | 请查看抗体网页的“灵敏度/特异度”部分。仅转染或重组抗体的灵敏度不足以检测靶标的内源性水平。内源性高灵敏度抗体适用于所有样品类型(内源性、转染或重组蛋白)。还可能需要增加或减少抗体用量,以获得最佳信号,具体取决于样品中的靶蛋白丰度。我们建议使用产品网页和数据表上显示的稀释度作为优化的起点。 另一个需要考虑的因素是抗体的物种反应性。CST 已对产品网页“反应性”部分列出的物种进行了内部验证。如果您的目的物种未列出,请联系我们的技术支持团队,他们将非常乐于帮助您确定抗体与您模型物种的蛋白序列的预期反应性。 | |
不完全裂解 | 无论使用哪种裂解缓冲液,CST 都建议进行超声处理,以确保完全裂解和最大/一致的蛋白回收率。超声处理对于确保膜结合和细胞器(如胞核和线粒体)靶标的高效蛋白提取是必不可少的,并且还用于剪切会干扰 SDS-PAGE 凝胶上样的胞核 DNA。建议使用探头超声波仪进行最佳的样品制备。对于 1 mL 样品,最佳处理方式为:在冰上用微型探头超声波破碎仪以 15W(或 50% 功率)进行 3 x 10 秒的脉冲超声处理。不过,也有效果良好的备选方法:将样本反复通过细规格针头(例如 24 号针头),或是用玻璃珠涡旋振荡处理。超声处理后,对样品进行离心分离,使不溶性细胞碎片和用于蛋白印迹实验的上清液沉淀。 | |
缓冲液选择不当 | 要使用单独抗体获得最佳结果,请参阅产品网页上的蛋白免疫印迹实验步骤,了解推荐的一抗稀释缓冲液(即 BSA 或奶粉)。如果没有用推荐的稀释缓冲液孵育抗体,可能会严重损害结果的灵敏度/特异度。例如,用脱脂奶粉孵育我们的许多一抗,条件过于严苛。一般而言,CST 建议使用 1X TBS/0.1% Tween-20/5% 脱脂奶粉进行封闭和二抗孵育,以尽量减少非特异性背景。使用其他封闭剂,如明胶、血清、无蛋白封闭剂、酪蛋白、或混合封闭剂,可能降低靶标信号强度。 许多客户对使用脱脂奶粉作为稀释缓冲液来检测磷酸化蛋白表示担心。具体而言,人们认为奶粉中的酪蛋白会导致背景较高。在 CST,我们在使用脱脂奶粉检测磷酸化蛋白时未发现任何问题。所有 CST 抗体在放行前均用 5% 脱脂奶粉和 5% BSA 进行了测试,最终将筛选出的最佳稀释缓冲液作为推荐方案。 封闭、抗体孵育(一抗和二抗)和洗涤缓冲液均应加入 1X TBS/0.1% Tween-20。较高或较低百分比的 Tween-20 会影响结果的灵敏度/特异度。使用 PBS 而非 TBS 可能会削弱我们某些抗体的信号强度。 | |
转移条件不当 | 我们通常建议用 25 mM Tris、192 mM 甘氨酸和 20% 甲醇在 4°C 下以 70 V (200-250 mA) 进行湿法转膜,持续 2 小时。但对于高分子量蛋白,我们建议将转膜缓冲液中的甲醇含量降至 5-10%,并将 70 V 下的转膜时间延长至 3-4 小时 (200-250 mA)。对于半干式转移,请参阅系统制造商的建议。 对于低分子量蛋白,务必要避免过转移或透膜流失(小靶标)。我们建议缩短转膜时间,并使用孔径为 0.2 μm 的硝酸纤维素转移膜,以最大程度减少低分子量(即小于 25-30 kDa)蛋白的流失。 | |
多个条带或非特异性结合 | 同工型反应性 | 某些细胞系和组织模型可以包含多种蛋白同工型或剪接变体,它们可以不同的分子量迁移。请参阅抗体网页上的“特异度/灵敏度”部分,确定是否预测或确认可检测到多种同工型。还可以在 UniProt 上查阅目的蛋白,看看是否列出了多个同工型序列。 |
翻译后修饰 | 翻译后修饰 (PTM) 会导致部分靶蛋白的电泳速率与未修饰蛋白不同。因此,诱导或抑制某些翻译后修饰的处理条件会导致在蛋白印迹中观察到多个条带。糖基化、SUMO 化、泛素化和磷酸化便是修饰的例子,这些修饰可能导致蛋白印迹上出现多个条带,但具体取决于使用的样品和处理方法。如果您正在查找更多靶蛋白相关的 PTM 信息,请参阅 PhosphoSitePlus。 | |
组织样品 | 组织样品是非均质的(即由不同细胞类型组成),因此使用在细胞系等其他样品类型中无法检测到的抗体时,出现非特异性条带的几率增加。此外,某些组织模型可能含有多种蛋白同工型或剪接变体,它们可以不同的分子量迁移。 | |
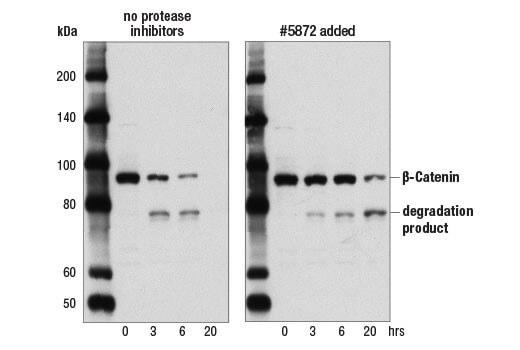
裂解物降解 | 样品中的蛋白酶和磷酸酶会快速降解蛋白。往裂解物中添加蛋白酶和磷酸酶抑制剂,有助于减缓或防止蛋白降解。我们建议往裂解缓冲液中加入亮抑酶肽(最终浓度为 1.0 μg/ml)和PMSF (#8553) 作为蛋白酶抑制剂。还可以使用 Protease Inhibitor Cocktail (100X) (#5871) 或 Protease/Phosphatase Inhibitor Cocktail (100X) (#5872)。 裂解物的长时间存放还可导致蛋白降解物增加,而蛋白降解物会通过抗体检测到。确保使用新鲜样品,以最大程度减少蛋白降解。在同一瓶样品中,某些蛋白的稳定性不如其他蛋白,因此,尽管一个样品可能对一个蛋白靶标有效,但同一样品中可能已经有不同的蛋白降解。 | |
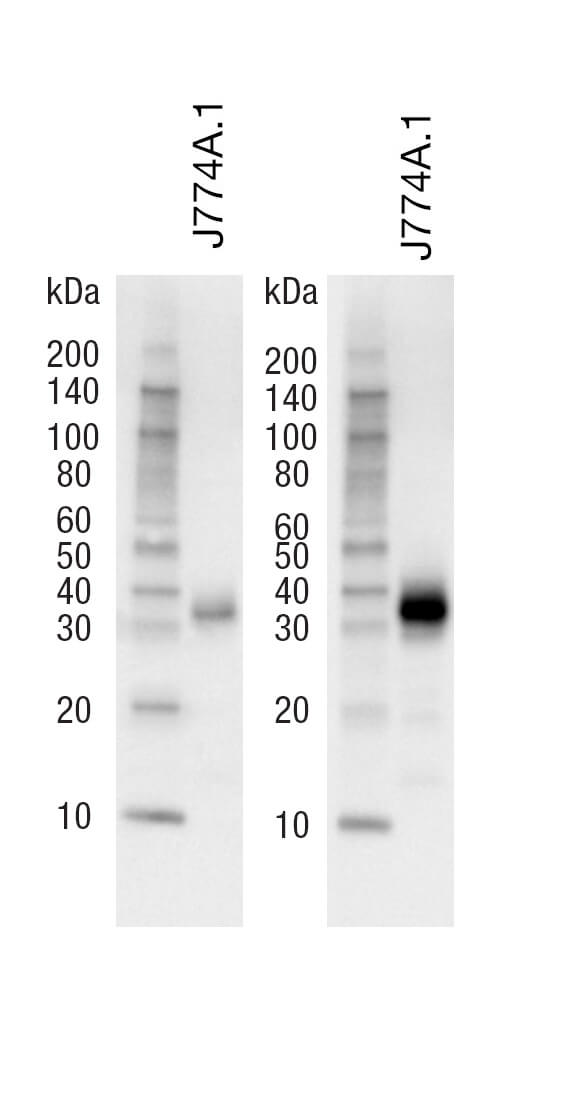
高蛋白浓度 | 如果使用高灵敏度抗体,膜上过量的蛋白会导致出现多个条带和高背景,且整个泳道中的信号强烈,而这些是蛋白量较少时不会存在的。尝试上样更少的蛋白,以观察更清晰的信号。 | |
曝光时间长 | 如果蛋白上样量太少,这会导致难以检测到目的蛋白,尤其是在样本类型中丰度较低的情况下。这反过来会导致需要延长曝光时间,以检测印迹上的靶蛋白。同时使用常见的 ECL 试剂时,CST 抗体经配制可在两分钟的曝光时间内产生信号。如果在该时间段内未观察到信号,则可能需要更高的蛋白浓度。 | |
一抗稀释缓冲液选择不当 | 一抗稀释缓冲液会影响膜背景。例如,与 BSA 相比,缓冲液(如脱脂奶粉)在减少印迹上出现非特异性条带和总背景方面将起到更好的作用。但奶粉对于某些抗体而言可能过于严苛,会导致靶标信号减弱。请务必参考 CST 产品网页上推荐的蛋白免疫印迹实验步骤,选择合适的一抗稀释缓冲液(即 BSA 或脱脂奶粉)。一般而言,CST 建议使用 1X TBS/0.1% Tween-20/5% 脱脂奶粉进行封闭和二抗孵育,以尽量减少非特异性背景。 | |
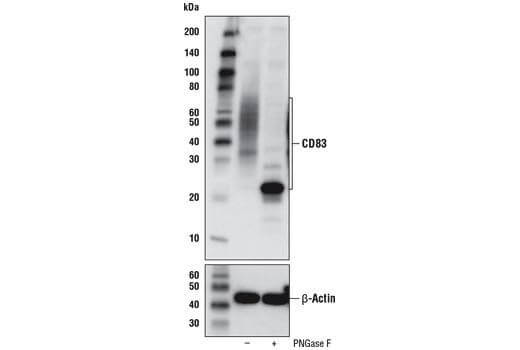
拖尾效应 | 糖基化蛋白 | 差异糖基化通常导致在分子量高于预测的分子量时产生条带拖尾效应。靶蛋白中糖基化的潜在位点可见于 PhosphoSitePlus。样品用一种使糖蛋白裂解 N-聚糖的酶 (PNGase F) 也可确认糖基化引起的分子量变化。 |
裂解物降解 | 样品中的蛋白酶和磷酸酶会快速降解蛋白。往裂解物中添加蛋白酶和磷酸酶抑制剂,有助于减缓或防止蛋白降解。我们建议往裂解缓冲液中加入亮抑酶肽(最终浓度为 1.0 μg/ml)和 PMSF (#8553) 作为蛋白酶抑制剂。还可以使用 Protease Inhibitor Cocktail (100X) (#5871) 或 Protease/Phosphatase Inhibitor Cocktail (100X) (#5872)。 裂解物的长时间存放还可导致蛋白降解物增加,而蛋白降解物会通过抗体检测到,在分子量低于预期的靶标分子量时出现拖尾效应。确保使用新鲜样品,以最大程度减少蛋白降解。如果需要长期储存,我们建议将裂解物储存在 -80°C,以减少降解。在同一瓶样品中,某些蛋白的稳定性不如其他蛋白,因此,尽管一个样品可能对一个蛋白靶标有效,但同一样品中可能已经有不同的蛋白降解。 | |
不完全裂解 | 无论使用哪种裂解缓冲液,CST 都建议进行超声处理,以确保完全裂解和最大/一致的蛋白回收率。超声处理对于确保膜结合和细胞器(如胞核和线粒体)靶标的高效蛋白提取是必不可少的,并且还用于剪切会干扰 SDS-PAGE 凝胶上样的胞核 DNA。建议使用探头超声波仪进行最佳的样品制备。对于 1 mL 样品,最佳处理方式为:在冰上用微型探头超声波破碎仪以 15W(或 50% 功率)进行 3 x 10 秒的脉冲超声处理。不过,也有效果良好的备选方法:将样本反复通过细规格针头(例如 24 号针头),或是用玻璃珠涡旋振荡处理。超声处理后,对样品进行离心分离,使不溶性细胞碎片和用于蛋白印迹实验的上清液沉淀。 | |
深色或黑色印迹 | 高浓度二抗 | 过量使用二抗(即辣根过氧化物酶)且配合高灵敏度的检测试剂 [如我们的 SignalFire™ Elite ECL Reagent (#12757)] 时,最常导致印迹发黑(无论是否出现白色“重影”条带)的现象。解决该问题的最佳方法是增加 HRP 偶联二抗的稀释比例(例如,从 1:2000 改为 1:10,000)。 |
洗涤不充分 | 洗涤时间缩短可能致使过多抗体残留在膜上,导致化学发光曝光后形成暗印迹。CST 建议在用一抗和二抗孵育后,用 1X TBS/0.1% Tween-20 常温洗涤三次,每次五分钟,以获得最佳的结果。 | |
缓冲液选择不当 | 使用封闭缓冲液以及是否加入其他洗涤剂均会影响膜背景。例如,与 BSA 相比,缓冲液(如脱脂奶粉)在减少印迹上出现非特异性条带和总背景方面将起到更好的作用。但奶粉对于某些抗体而言可能过于严苛,会导致靶标信号减弱。请务必参考产品网页上推荐的蛋白免疫印迹实验步骤,为一抗孵育选择适当的稀释缓冲液(即 BSA 或脱脂奶粉)。一般而言,CST 建议使用 1X TBS/0.1% Tween-20/5% 脱脂奶粉进行封闭和二抗孵育,以最大程度减少非特异性背景。 | |
膜复水 | 为了获得最佳性能,我们建议直接将硝酸纤维素膜放在转移缓冲液中复水。但使用 PVDF 时,在将膜移至转移缓冲液之前,应将膜放在甲醇中短暂复水。 | |
散斑或斑点样印迹 | 转移海绵污染 | 长时间未经过适当消毒的转移海绵可能含有细菌污染物。要排除这个因素,请使用新的转移海绵。 |
缓冲液污染 | 超过几天的缓冲液可能有更多细菌和真菌污染物,这些污染物会导致膜上出现斑点。我们建议始终使用新鲜配制的缓冲液,以获得最佳效果。 |